2. ต่อแอมมิเตอร์ชนิดที่นำไฟฟ้าได้เป็นไมโครแอมแปร์เข้ากับเครื่องตรวจการนำไฟฟ้า แล้วจุ่มลวดตัวนำของเครื่องตรวจการนำไฟฟ้าลงในน้ำกลั่น ดังรูป อ่านค่ากระแสไฟฟ้า บันทึกผล
3. อุ่นน้ำกลั่นให้ร้อนประมาณ 60 cแล้วทดสอบการนำไฟฟ้าเช่นเดียวกับข้อ 2
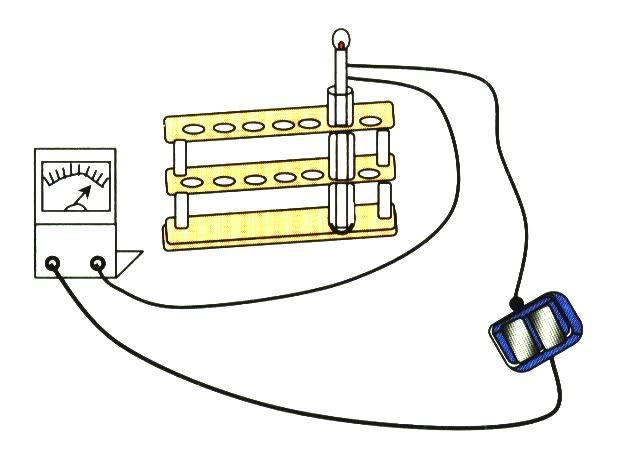 ผลการทดลอง
ผลการทดลองน้ำบริสุทธิ์นำไฟฟ้าได้น้อยมาก จนไม่สามารถตรวจสอบได้ดัวยเครื่องตรวจการนำไฟฟ้าธรรมดา แต่เมื่อใช้แอมมิเตอร์ช่วยในการทดสอบ เข็มของแอมมิเตอร์เบนเล็กน้อย แสดงว่าน้ำบริสุทธิ์แตกตัวให้ไฮโดรเนีบมไอออนและไฮดรอกไซด์ไอออนน้อยมาก การแตกตัวของน้ำบริสุทธิ์เป็นดังสมการ
H2O(l)+ H2O(l)  H3O+(aq) +OH- (aq)
H3O+(aq) +OH- (aq)
K[H2O]2 = [H3O+][OH-]
เนื่องจากน้ำแตกตัวได้น้อยมากจนถือว่าความเข้มข้นของน้ำไม่เปลี่ยนแปลง เมื่อจัดความสัมพันธ์อยู่ในรูปใหม่ จึงได้ค่าคงที่ใหม่ซึ่งเรียกว่า ค่าคงที่การแตกตัวของน้ำ ใช้สัญลักษณ์ Kw
ดังนั้นKw= [H3O+][OH-]
จากผลการทดลอง พบว่าน้ำที่อุณหภูมิสูงนำไฟฟ้าได้ดีกว่าที่อุณหภูมิต่ำ แสดงว่าน้ำที่อุณหภูมิสูงแตกตัวเป็นไอออนได้มากกว่าที่อุณหภูมิต่ำKwจึงสูงกว่า ตัวอย่างเช่น
ค่า ที่อุณหภูมิ 25cมีค่าเท่ากับ 1.0 x 10-14mol/dm3
ค่า ที่อุณหภูมิ 60 cมีค่าเท่ากับ 9.5 x 10-14mol/dm3
ดังนั้น การบอกค่าKwจึงต้องระบุอุณหภูมิด้วยเช่นเดียวกับค่าคงที่อื่นๆ โดยปกติเราไม่กล่าวถึงหน่วยของ Kwเช่นเดียวกับค่าคงที่สมดุลอื่นๆ ยกเว้นในกรณีที่จะนำมาใช้คำนวณความเข้มข้นของไอออนที่ระบุหน่วยของ Kw
จากสมการการแตกตัวของน้ำ จะได้ไฮโดรเนียมไอออนและไฮดรอกไซด์ไอออนเกิดขึ้นในจำนวนโมลที่เท่ากัน ดัวนั้น
=[OH- ]นั่นคือKw=[H3O+]2หรือ [OH-]2
[H3O+] หรือ[H3O+] =[OH-] =Kw
=[OH-] =1.0 x 10-14 mol2/dm6 ณ อุณหภูมิ 25 c
[H3O+] =1.0 x 10-7 mol/dm3
แสดงว่าน้ำบริสุทธิ์ที่อุณหภูมิ 25 cมีความเข้มข้นของไฮดรอกไซด์ไอออน คือ1.0 x 10-7
ไม่มีความคิดเห็น:
แสดงความคิดเห็น